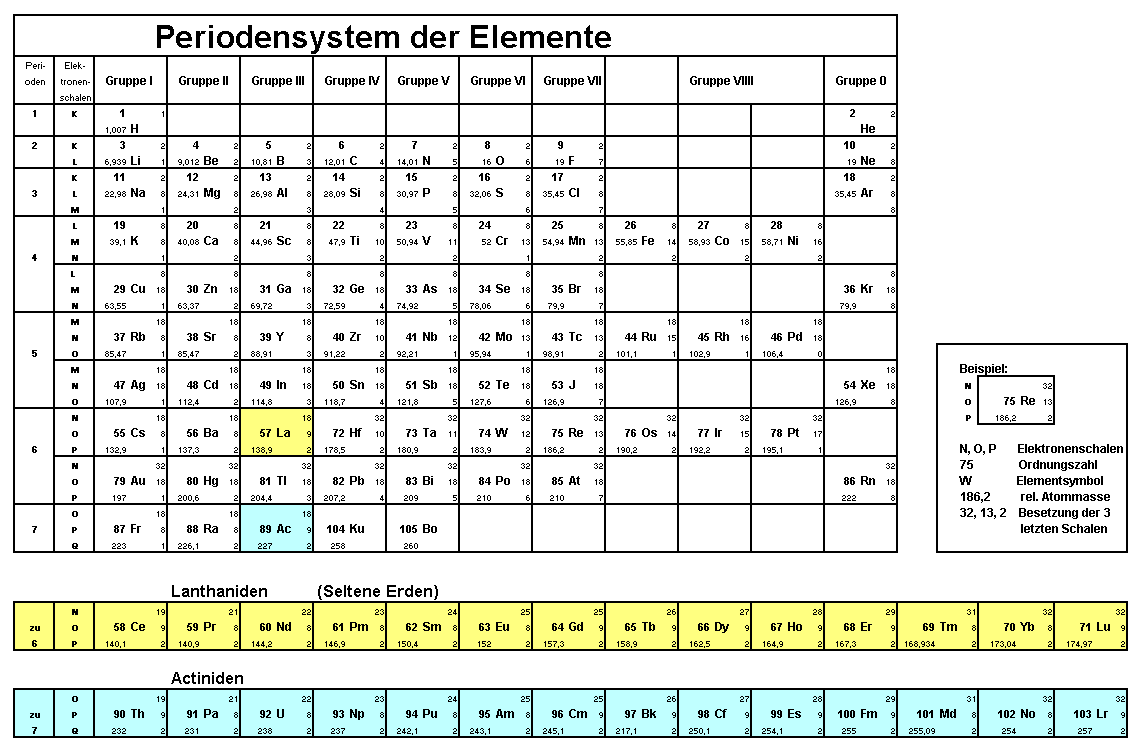
Im Periodensystem werden 105 chemische Elemente in einem sinnvollen System dargestellt. Diejenigen
Elemente, die senkrecht untereinander angeordnet sind (Gruppe), haben z.B. alle dieselbe Elektronenzahl
in der äusseren Schale. Diese Zahl bestimmt im Wesentlichen die chemischen Eigenschaften, also welches Element mit
welchem anderen chemische Verbindungen eingeht. Daher haben alle Elemente einer Gruppe ähnliche chemische
Eigenschaften.
Alle horizontal nebeneinanderstehende (Periode) Elemente haben im Normalzustand gleich viele Schalen,
auf denen sich Elektronen befinden.
Heutzutage kennt man etwa 114 verschiedene Elemente. Spezielle Institute der Grundlagenforschung bemühen sich ständig noch
schwerere Atome zu "bauen". Alle diese bisher künstlich erzeugten schweren Elemente zerfallen jedoch in extrem kurzer Zeit
(radioaktiv), so dass sie für die Technik bisher nicht nutzbar sind.
Elemente sind Stoffe, deren Atome bis auf die Neutronenzahl alle gleich sind, daher gleiche chemische Eigenschaften haben bzw. mit
Methoden der Chemie nicht voneinander unterscheidbar sind. So haben z.B. alle Cu-Atome genau 29
Protonen und auch genau 29 Elektronen. Darunter gibt es einige mit 34 Neutronen aber
auch welche mit 36 Neutronen (verschiedene Isotope).
Künstlich kann man sogar Cu-Atome erzeugen mit noch etwas mehr oder etwas weniger Neutronen. Diese Atome sind aber alle radioaktiv
und zerfallen von selbst nach einer gewissen Zeit unter Aussendung radioaktiver Strahlung.
Die Legende zum Periodensystem findet man unten rechts im Periodensystem (Bild nach links schieben). Hier noch einige Erläuterungen:
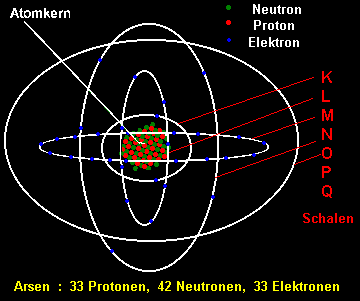
1. Die Bezeichnung der Elektronenschalen werden im Kapitel Bohrsches Atommodell
erklärt.
2. Die Ordnungszahl ist sowohl die fortlaufende Nummerierung der Atome, gibt aber auch die Protonenzahl
im Kern bzw. die Zahl der Elektronen auf den Schalen des Atoms an.
3. Das Elementsymbol ist die international gebräuchliche Abkürzung des Atomnamens.
4. Mutipliziert man die relative Atommasse mit 1,66 * 10 -27kg, so erhält
man die absolute Atommasse.
5.Die Besetzungszahlen geben an, wieviele Elektronen normalerweise auf den jeweiligen Schalen
sind.
 Während das ausführliche Periodensystem oben einige Daten der Elemente bietet, zeigt das untere Bild die
Aggregatzustände der Atome im Normalzustand (= 1 bar Druck und 0 &# 1455;C Umgebungsbedingungen)
Während das ausführliche Periodensystem oben einige Daten der Elemente bietet, zeigt das untere Bild die
Aggregatzustände der Atome im Normalzustand (= 1 bar Druck und 0 &# 1455;C Umgebungsbedingungen)
Alle grün oder blau geschriebenen Atome sind radioaktiv. Alle anderen Elemente sind stabil, d.h. sie zerfallen nicht und
senden keine radioaktive Strahlung aus. Allerdings kann man durch z.B. Bestrahlung auch aus diesen
natürlicherweise stabilen Atomen radioaktive machen.
Unter den Elementen sind nur etwa 20 Nichtmetalle, alle anderen sind Metalle.
| Atomsymbol |
Atomname |
Ordnungszahl |
rel. Atommasse |
Entdeckungsjahr |
Dichte |
Schmelztemperatur |
Siedetemperatur |
| . |
. |
. |
. |
. |
g/cm3 |
&# 1455;C |
&# 1455;C |
| Ac |
Actinium |
89 |
227 |
1899 |
. |
. |
. |
| Ag |
Silber |
47 |
107,88 |
. |
10,5 |
961,3 |
2180 |
| Al |
Aluminium |
13 |
26,9815 |
1827 |
2,698 |
69 |
2447 |
| Am |
Americum |
95 |
243? |
1945 |
. |
. |
. |
| Ar |
Argon |
218 |
39,984 |
1894 |
0,178 |
-189,3 |
-185,87 |
| As |
Arsen |
33 |
74,9216 |
. |
5,72 |
815 |
613 |
| At |
Astat |
85 |
210? |
1940 |
. |
. |
. |
| Au |
Gold |
79 |
196,967 |
. |
19,3 |
1064,76 |
2707 |
| B |
Bor |
5 |
10,811 |
1808 |
2,33 |
2030 |
3900 |
| Ba |
Barium |
56 |
137,34 |
1808 |
3,61 |
710 |
1637 |
| Be |
Beryllium |
4 |
9,122 |
1798 |
1,86 |
1283 |
2477 |
| Bh |
Bohrium |
107 |
262,1229 |
. |
. |
. |
. |
| Bi |
Wismuth |
83 |
208,98 |
1753 |
9,79 |
271 |
1560 |
| Bk |
Berkelium |
97 |
249? |
1950 |
. |
. |
. |
| Br |
Brom |
35 |
79,909 |
1826 |
3,14 |
-8,25 |
58,2 |
| C |
Kohlenstoff |
6 |
12,1115 |
. |
2,2 |
3800 |
4000 |
| Ca |
Calcium |
20 |
40,8 |
1808 |
1,54 |
850 |
1487 |
| Cd |
Cadmium |
48 |
112,40 |
1817 |
8,642 |
321 |
765 |
| Ce |
Cer |
58 |
140,12 |
1803 |
6,768 |
797 |
3470 |
| Cf |
Californium |
98 |
251? |
1950 |
. |
. |
. |
| Cl |
Chlor |
17 |
35,453 |
1774 |
0,178 |
-101 |
10,44 |
| Cm |
Curium |
96 |
247? |
1944 |
. |
. |
. |
| Co |
Kobalt |
27 |
58,9332 |
1735 |
8,9 |
1493 |
2880 |
| Cr |
Chrom |
24 |
51,996 |
1797 |
7,2 |
1903 |
2642 |
| Cs |
Cäsium |
55 |
132,905 |
1860 |
1,873 |
28,64 |
685 |
| Cu |
Kupfer |
29 |
63,54 |
. |
8,96 |
1083 |
2595 |
| Db |
Dubnium |
105 |
262,1138 |
. |
. |
. |
. |
| Dy |
Dysprosium |
66 |
132,50 |
1886 |
8,559 |
1407 |
2330 |
| Er |
Erbium |
68 |
167,26 |
1843 |
9,62 |
1497 |
2420 |
| Es |
Einsteinium |
99 |
. |
1955 |
. |
. |
. |
| Eu |
Europium |
63 |
151,96 |
1896 |
5,24 |
826 |
1430 |
| F |
Fluor |
9 |
18,9984 |
1771 |
0,1696 |
-218 |
-188,1 |
| Fe |
Eisen |
26 |
55,847 |
. |
7,87 |
1536 |
3070 |
| Fm |
Fermium |
100 |
. |
1955 |
. |
. |
. |
| Fr |
Francium |
87 |
223? |
1993 |
. |
. |
. |
| Ga |
Gallium |
31 |
69,72 |
1875 |
5,91 |
29,78 |
2227 |
| Gd |
Gadolinium |
64 |
157,25 |
1880 |
7,886 |
1312 |
2800 |
| Ge |
Germanium |
32 |
72,59 |
1886 |
5,33 |
937,2 |
2830 |
| H |
Wasserstoff |
1 |
1,797 |
1766 |
0,301 |
-259,2 |
-252,76 |
| He |
Helium |
2 |
4,26 |
1895 |
0,6945 |
-269,7 |
-268,94 |
| Hf |
Hafnium |
72 |
178,49 |
1923 |
13,36 |
2220 |
5200 |
| Hg |
Quecksiber |
80 |
200,59 |
. |
13,55 |
-38,86 |
356,73 |
| Ho |
Holmium |
67 |
164,93 |
1879 |
8,8 |
1461 |
2490 |
| Hs |
Hassium |
108 |
269,13 |
. |
. |
. |
. |
| In |
Indium |
49 |
114,82 |
1863 |
7,3 |
156,17 |
2047 |
| Ir |
Iridium |
77 |
192,2 |
1803 |
22,4 |
2443 |
4350 |
| J |
Jod |
53 |
126,9044 |
1811 |
4,932 |
113,6 |
182,8 |
| K |
Kalium |
19 |
39,102 |
1807 |
0,862 |
63,2 |
753,8 |
| Kr |
Krypton |
36 |
83,80 |
1898 |
0,3744 |
-157,2 |
-153,2 |
| La |
Lanthan |
57 |
138,91 |
1839 |
6,162 |
920 |
3470 |
| Li |
Lithium |
3 |
6,939 |
1817 |
0,534 |
180,5 |
1317 |
| Lr |
Lawrencium |
103 |
260,1053 |
. |
. |
. |
. |
| Lu |
Lutetium |
71 |
174,97 |
1907 |
9,85 |
1652 |
3000 |
| Md |
Mendelevium |
101 |
. |
1955 |
. |
. |
. |
| Mg |
Magnesium |
12 |
24,312 |
1755 |
1,741 |
649,5 |
1120 |
| Mn |
Mangan |
25 |
54,938 |
1774 |
7,43 |
1244 |
2095 |
| Mo |
Molybdän |
42 |
95,94 |
1778 |
10,22 |
2620 |
4800 |
| Mt |
Meitnerium |
109 |
268,14 |
. |
. |
. |
. |
| N |
Stickstoff |
7 |
14,67 |
1772 |
0,311 |
-210 |
-195,81 |
| Na |
Natrium |
11 |
22,9898 |
1807 |
0,971 |
97,82 |
890 |
| Nb |
Niob |
41 |
92,906 |
1801 |
8,55 |
2468 |
4900 |
| Nd |
Neodym |
60 |
144,24 |
1885 |
7,7 |
1020 |
3210 |
| Ne |
Neon |
10 |
20,183 |
1898 |
0,4835 |
-248,6 |
-246,1 |
| Ni |
Nickel |
28 |
58,71 |
1751 |
8,91 |
1455 |
2800 |
| No |
Nobelium |
102 |
. |
1958 |
. |
. |
. |
| Np |
Neptunium |
93 |
237? |
1940 |
. |
. |
. |
| O |
Sauerstoff |
8 |
15,9994 |
1774 |
0,419 |
-218,81 |
-183,0 |
| Os |
Osmium |
76 |
190,2 |
1803 |
22,43 |
2700 |
4400 |
| P |
Phosphor |
15 |
30,9738 |
1669 |
2,69 |
44,2 |
281 |
| Pa |
Protactinium |
91 |
231? |
1917 |
. |
. |
. |
| Pb |
Blei |
82 |
207,19 |
. |
11,337 |
327,4 |
1751 |
| Pd |
Paladium |
46 |
106,4 |
1803 |
12,1 |
1550 |
3560 |
| Pm |
Promethium |
61 |
145? |
1947 |
. |
1035 |
3200 |
| Po |
Polonium |
84 |
210? |
1898 |
. |
. |
. |
| Pr |
Praseodym |
59 |
140,907 |
1879 |
6,77 |
935 |
3017 |
| Pt |
Platin |
78 |
195,9 |
1735 |
21,5 |
1769 |
4300 |
| Pu |
Plutonium |
94 |
242? |
1940 |
. |
. |
. |
| Ra |
Radium |
88 |
226,5 |
1898 |
. |
. |
. |
| Rb |
Rubidium |
37 |
85,47 |
1861 |
1,532 |
38,7 |
701 |
| Re |
Rhenium |
75 |
186,2 |
1925 |
21,4 |
3180 |
5600 |
| Rf |
Rutherfordium |
104 |
261,1087 |
. |
. |
. |
. |
| Rh |
Rhodium |
45 |
102,905 |
1803 |
12,5 |
1960 |
3960 |
| Rn |
Radon |
86 |
222? |
1900 |
. |
. |
. |
| Ru |
Ruthetium |
44 |
101,7 |
1844 |
12,3 |
2500 |
4110 |
| S |
Schwefel |
16 |
32,64 |
. |
2,7 |
115,18 |
444,6 |
| Sb |
Antimon |
51 |
121,75 |
. |
18,22 |
630,5 |
1637 |
| Sc |
Scandium |
21 |
44,956 |
1879 |
2,99 |
1538 |
2730 |
| Se |
Selen |
34 |
78,96 |
1817 |
4,79 |
217,4 |
684,9 |
| Sg |
Seaborgium |
106 |
263,1182 |
. |
. |
|
|
| Si |
Silizium |
14 |
28,86 |
1823 |
2,326 |
1423 |
2355 |
| Sm |
Samarium |
62 |
150,35 |
1879 |
7,53 |
1072 |
1670 |
| Sn |
Zinn |
50 |
118,69 |
. |
7,29 |
231,9 |
2687 |
| Sr |
Strontium |
38 |
87,62 |
1790 |
2,67 |
770 |
1367 |
| Ta |
Tantal |
73 |
180,948 |
1802 |
16,6 |
2996 |
5400 |
| Tb |
Terbium |
65 |
158,924 |
1843 |
8,253 |
1356 |
2800 |
| Tc |
Technetium |
43 |
99? |
1937 |
. |
. |
. |
| Te |
Tellur |
52 |
127,60 |
1782 |
6,25 |
449,5 |
989,8 |
| Th |
Thorium |
90 |
232,38 |
1828 |
11,7 |
1695 |
4200 |
| Ti |
Titan |
22 |
47,90 |
1791 |
4,505 |
1668 |
3280 |
| Tl |
Thallium |
81 |
204,37 |
1861 |
11,85 |
303,5 |
1457 |
| Tm |
Thulium |
69 |
168,934 |
1879 |
18,13 |
1545 |
1720 |
| U |
Uran |
92 |
238,3 |
1789 |
19,1 |
1130 |
3930 |
| Uun |
Ununnilium |
110 |
269,3 |
. |
. |
. |
. |
| Uuu |
Unununium |
111 |
272 |
. |
. |
. |
. |
| Cp (Cn?) |
Copernicum |
112 |
278 |
1996 |
. |
. |
. |
| V |
Vanadium |
23 |
50,942 |
1830 |
6,12 |
1800 |
3380 |
| W |
Wolfram |
74 |
183,85 |
1781 |
19,27 |
3390 |
5500 |
| Xe |
Xenon |
54 |
131,30 |
1898 |
0,11 |
-111,9 |
-108,1 |
| Y |
Yttrium |
39 |
88,905 |
1794 |
4,472 |
1500 |
3630 |
| Yb |
Ytterbium |
70 |
173,4 |
1878 |
6,96 |
824 |
1520 |
| Zn |
Zink |
30 |
65,37 |
1746 |
7,13 |
419,5 |
907 |
| Zr |
Zirkon |
40 |
91,22 |
1789 |
6,5 |
1855 |
4380 |
Quelle: Dans-Lax,1967
Viele weitere Informationen zum Periodensystem, Atombau, Daten der Elemente ... finden Sie unter
/le-village.ifrance.com/okapi/periodensystem.htm
oder
www.uniterra.de
oder
www.seilnacht.tuttlingen.com


 Während das ausführliche Periodensystem oben einige Daten der Elemente bietet, zeigt das untere Bild die
Aggregatzustände der Atome im Normalzustand (= 1 bar Druck und 0 &# 1455;C Umgebungsbedingungen)
Während das ausführliche Periodensystem oben einige Daten der Elemente bietet, zeigt das untere Bild die
Aggregatzustände der Atome im Normalzustand (= 1 bar Druck und 0 &# 1455;C Umgebungsbedingungen)